Kierownik projektu
:
Dr hab. Barbara Kutryb-Zając, prof. GUMed
Gdański Uniwersytet Medyczny
Panel: NZ4
Konkurs
: OPUS 26
ogłoszony
18 września 2023
Choroby sercowo-naczyniowe, w tym niewydolność serca, pozostają jedną z głównych przyczyn zachorowalności i zgonów w krajach rozwiniętych. Coraz więcej danych wskazuje, że jednym z kluczowych, a wciąż niedostatecznie poznanych mechanizmów leżących u podłoża ich rozwoju jest dysfunkcja śródbłonka naczyniowego, która często pojawia się na bardzo wczesnym, przedklinicznym etapie choroby. Komórki śródbłonka, wyścielające światło wszystkich naczyń krwionośnych i stanowiące niemal wyłączny element strukturalny mikrokrążenia, tworzą wysoce aktywną metabolicznie i sygnałowo warstwę regulującą napięcie naczyń, przepływ krwi, hemostazę, odpowiedź zapalną oraz wymianę tlenu i metabolitów w tkankach. Zaburzenie tych funkcji prowadzi w pierwszej kolejności do upośledzenia mikrokrążenia, co skutkuje niedostatecznym zaopatrzeniem tkanek w składniki odżywcze, nasileniem stresu oksydacyjnego i stanu zapalnego, a w konsekwencji inicjuje procesy patologiczne prowadzące do progresji niewydolności serca.
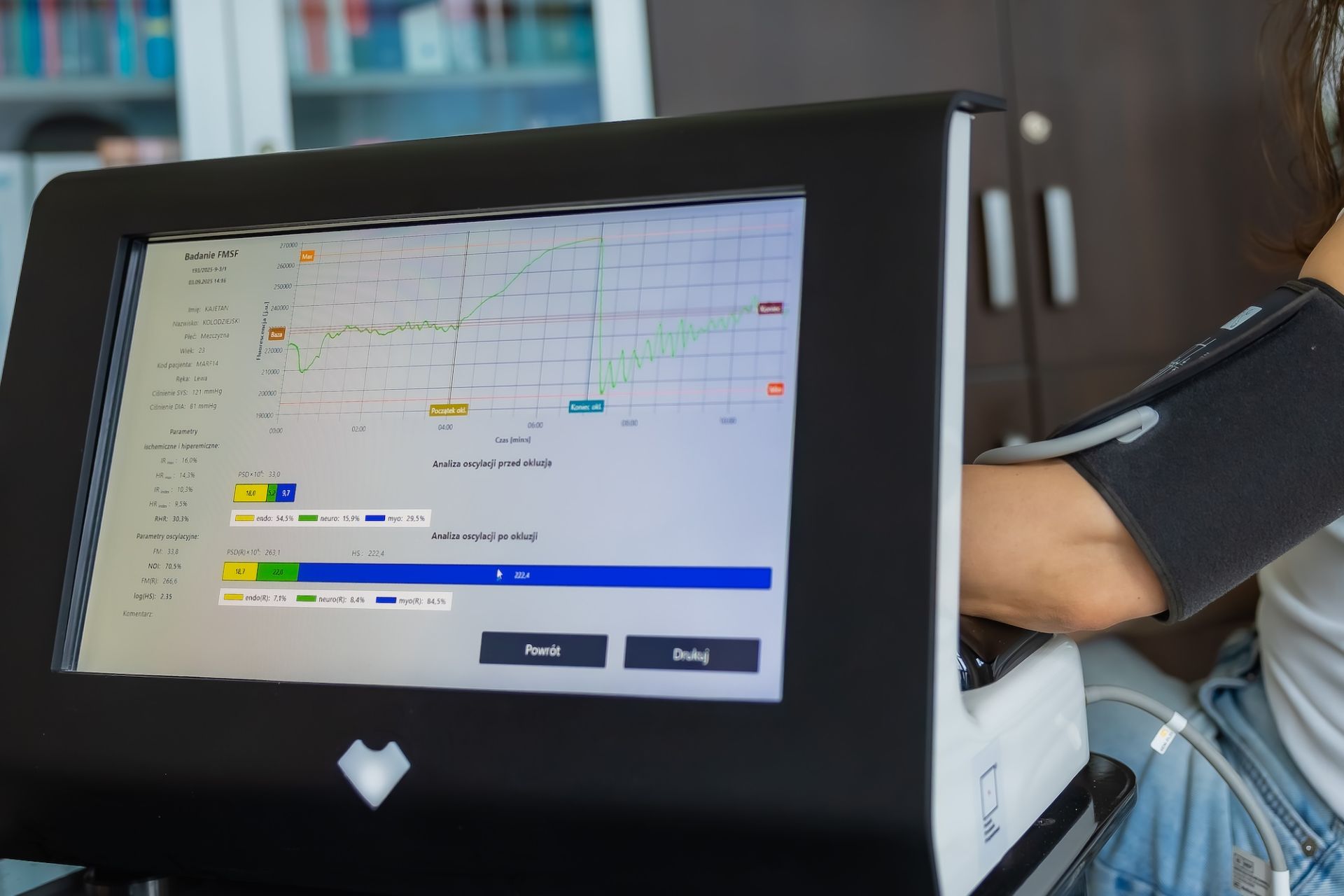 Aparat do nieinwazyjnej oceny funkcji mikrokrążenia obwodowego. Fot. Paweł Sudara
Aparat do nieinwazyjnej oceny funkcji mikrokrążenia obwodowego. Fot. Paweł Sudara
Dysfunkcja śródbłonka mikrokrążenia jest obecnie uznawana za funkcjonalny prekursor późniejszych zmian strukturalnych w większych naczyniach, w tym procesu miażdżycowego oraz za istotny czynnik determinujący przebieg niewydolności serca niezależnie od etiologii choroby. Utrata zdolności śródbłonka do prawidłowej regulacji rozszerzania naczyń, przeciwdziałania rozwojowi procesów zapalnym i oksydacyjnym oraz wsparcia metabolizmu kardiomiocytów prowadzi do narastającej dysfunkcji narządowej, jeszcze zanim dojdzie do widocznych zmian anatomicznych w układzie naczyniowym. Z tego względu zrozumienie mechanizmów regulujących funkcję śródbłonka, zwłaszcza na poziomie mikrokrążenia, ma fundamentalne znaczenie nie tylko dla poznania patogenezy niewydolności serca, ale również dla opracowania strategii wczesnej diagnostyki oraz interwencji terapeutycznych, które mogą zahamować lub odwrócić rozwój choroby na etapie przedklinicznym.
Badania realizowane w ramach projektu obejmują zarówno analizy prowadzone u pacjentów z przewlekłą niewydolnością serca, jak i badania mechanistyczne z wykorzystaniem modeli eksperymentalnych in vitro oraz in vivo. Projekt koncentruje się na roli mitochondriów komórek śródbłonka w regulacji funkcji mikrokrążenia oraz na ocenie mitochondrialnych mechanizmów działania inhibitorów kotransportera sodowo-glukozowego (SGLT2i, tzw. flozyn) w śródbłonku naczyniowym. Takie podejście umożliwia bezpośrednie powiązanie obserwowanych efektów fizjologicznych z procesami zachodzącymi na poziomie subkomórkowym i molekularnym.
 Od lewej: mgr Iga Walczak, mgr Roksana Knapczyk i dr hab. Barbara Kutryb-Zając, prof. GUMed podczas przyżyciowego obrazowania mitochondriów w komórkach śródbłonka. Fot. Paweł Sudara
Od lewej: mgr Iga Walczak, mgr Roksana Knapczyk i dr hab. Barbara Kutryb-Zając, prof. GUMed podczas przyżyciowego obrazowania mitochondriów w komórkach śródbłonka. Fot. Paweł Sudara
Zastosowanie nowoczesnych metod badawczych, takich jak przyżyciowa rejestracja fluorescencji NADH w ludzkim naskórku jako testu do oceny aktywności śródbłonka naczyniowego i związanej z nią sprawności mikrokrążenia, w połączeniu z analizą krążących markerów dysfunkcji mitochondrialnej, stresu oksydacyjnego i stanu zapalnego, pozwala na integrację danych uzyskanych w modelach eksperymentalnych i badaniach u pacjentów kardiologicznych. Takie podejście sprzyja translacji wiedzy podstawowej w kontekście fizjologii i patofizjologii, przy jednoczesnym zachowaniu charakteru badań fundamentalnych.
W realizację projektu zaangażowany jest interdyscyplinarny zespół badaczy reprezentujących biochemię, biologię komórki, fizjologię, kardiologię kliniczną oraz diagnostykę obrazową. Taka struktura zespołu umożliwia wielopoziomową analizę problemu dysfunkcji śródbłonka – od mechanizmów molekularnych i mitochondrialnych, przez konsekwencje metaboliczne i naczyniowe, aż po ich manifestację w warunkach klinicznych.
Projekt realizowany jest w ścisłej współpracy jednostek Gdańskiego Uniwersytetu Medycznego, w tym Katedry i Zakładu Biochemii, Katedry i Zakładu Diagnostyki Chorób Serca oraz Centrum Kardioonkologii Doświadczalnej. Ponadto, w ramach konsorcjum, w badania zaangażowani są naukowcy z Centrum Medycznego Kształcenia Podyplomowego oraz Uniwersytetu Gdańskiego, co dodatkowo wzmacnia potencjał badawczy projektu.
Dotychczasowe wyniki badań dostarczyły istotnych informacji na temat roli mitochondriów w regulacji funkcji śródbłonka naczyniowego oraz pozwoliły na identyfikację nowych mechanizmów molekularnych istotnych w patogenezie niewydolności serca. Wykazano plejotropowe działanie flozyn na oddychanie mitochondrialne i plastyczność metaboliczną komórek śródbłonka. W dalszym etapie projektu planowane jest opracowanie nieinwazyjnego podejścia diagnostycznego, opartego na komplementarnej analizie funkcji mikrokrążenia obwodowego oraz metabolomicznej charakterystyce śródbłonka, co umożliwi wcześniejsze wykrywanie i monitorowanie zaburzeń sercowo-naczyniowych.
Projekt stanowi przykład nowatorskich badań podstawowych o wysokim potencjale translacyjnym, w których integracja kompetencji z zakresu nauk biomedycznych i klinicznych stwarza podstawy do lepszego zrozumienia mechanizmów chorób układu krążenia oraz do identyfikacji nowych kierunków rozwoju diagnostyki i terapii.
 Dr hab. Magdalena Narajczyk, prof. UG podczas analizy morfologii mitochondriów komórek śródbłonka z wykorzystaniem transmisyjnej mikroskopii elektronowej. Fot. Małgorzata Kapusta
Dr hab. Magdalena Narajczyk, prof. UG podczas analizy morfologii mitochondriów komórek śródbłonka z wykorzystaniem transmisyjnej mikroskopii elektronowej. Fot. Małgorzata Kapusta
 Od lewej: mgr Aleksandra Parzuchowska, dr Maria Tarnawska, prof. Marcin Hellmann prowadzący analizy u pacjentów z przewlekłą niewydolnością serca. Fot. Paweł Sudara
Od lewej: mgr Aleksandra Parzuchowska, dr Maria Tarnawska, prof. Marcin Hellmann prowadzący analizy u pacjentów z przewlekłą niewydolnością serca. Fot. Paweł Sudara
Pełny tytuł finansowanego projektu: Mitochondrialne działania flozyn w komórkach śródbłonka - nowe podejście do prewencji, diagnostyki i terapii niewydolności serca
Dr hab. Barbara Kutryb-Zając, prof. GUMed

Na zdjęciu: dr hab. Barbara Kutryb-Zając, prof. GUMed, kierownik projektu i prof. Marcin Hellmann, lider części klinicznej projektu. Fot. Paweł Sudara
Dr hab. Barbara Kutryb-Zając, prof. GUMed
Doktor habilitowany nauk medycznych, profesor uczelni na Wydziale Lekarskim Gdańskiego Uniwersytetu Medycznego oraz koordynator uczelnianego Centrum Kardioonkologii Doświadczalnej. Od 2018 roku zatrudniona w Katedrze i Zakładzie Biochemii GUMed. Laureatka Nagrody im. Witolda Drabikowskiego za najlepszą pracę doktorską z biochemii (2017). Kierownik projektów badawczych: Preludium (2016-2019) oraz Sonata (2020-2025). Beneficjentka grantu naukowego Polskiego Towarzystwa Kardiologicznego (2025). Koncentruje się na badaniach mechanizmów dysfunkcji śródbłonka naczyniowego, ze szczególnym uwzględnieniem patofizjologii układu sercowo-naczyniowego oraz zagadnień z pogranicza kardiologii i onkologii.
Prof. dr hab. Marcin Hellmann
Profesor nauk medycznych, specjalista kardiologii, kierownik Katedry i Zakładu Diagnostyki Chorób Serca GUMed. Specjalizuje się w badaniach nad mikrokrążeniem. Absolwent studiów Master of Science (cardiovascular and metabolic regulations) na Uniwersytecie Claude Bernard w Lyonie we Francji w 2011. W latach 2014-2015 odbył staż podoktorski w ośrodku badawczym INSERM na Uniwersytecie w Grenoble we Francji. Trzykrotny Stypendysta Rządu Francuskiego i Fundacji na rzecz Nauki Polskiej. Laureat Nagrody Naukowej Miasta Gdańska dla młodych naukowców im. Jana Uphagena (2015) oraz Stypendium Minstra Nauki i Szkolnictwa Wyższego dla wybitnych młodych naukowców (w lata 2016-2019).
 Dr hab. Michał Mączewski, prof. CMKP
Dr hab. Michał Mączewski, prof. CMKP
Profesor uczelni, kierownik Zakładu Fizjologii Klinicznej w Centrum Medycznego Kształcenia Podyplomowego. Jego badania koncentrują się na mechanizmach zaburzeń rytmu oraz patofizjologii niewydolności serca. Prowadzi badania eksperymentalne na modelach zwierzęcych oraz badania translacyjne i kliniczne dotyczące miażdżycy i choroby niedokrwiennej, realizowane we współpracy z licznymi ośrodkami naukowymi.
Fot. Aleksandra Paterek
 Dr Małgorzata Kapusta
Dr Małgorzata Kapusta
Doktor nauk biologicznych, prowadzi badania w Laboratorium Bioobrazowania na Wydziale Biologii Uniwersytetu Gdańskiego. Specjalizuje się w zaawansowanych technikach bioobrazowania, analizie procesów komórkowych oraz zastosowaniu metod mikroskopowych w badaniach biologicznych i biomedycznych.
Fot. Małgorzata Narajczyk